Стали важным шагом в развитии физики. Огромное значение имела модель Резерфорда. Атом как система и частицы, его составляющие, был изучен более точно и подробно. Это привело к успешному становлению такой науки, как ядерная физика.
Античные представления о строении вещества
Предположение о том, что окружающие тела состоят из мельчайших частиц, были высказаны еще в античные времена. Мыслители того времени представляли атом в виде мельчайшей и неделимой частицы любого вещества. Они утверждали, что нет во Вселенной ничего меньшего по размеру, чем атом. Таких взглядов придерживались великие древнегреческие ученые и философы - Демокрит, Лукреций, Эпикур. Гипотезы этих мыслителей сегодня объединены под названием «античный атомизм».
Средневековые представления
Времена античности прошли, и в средние века также были ученые, которые высказывали различные предположения о строении веществ. Однако преобладание религиозных философских взглядов и власть церкви в тот период истории на корню пресекали любые попытки и стремления человеческого разума к материалистическим научным выводам и открытиям. Как известно, средневековая инквизиция весьма недружелюбно вела себя с представителями научного мира того времени. Остается сказать, что у тогдашних светлых умов было пришедшее из античности представление о неделимости атома.
Исследования 18-19 веков
18 столетие было отмечено серьезными открытиями в области элементарного строения вещества. Во многом благодаря стараниям таких ученых, как Антуан Лавуазье, Михаил Ломоносов и Независимо друг от друга они сумели доказать, что атомы действительно существуют. Но вопрос об их внутреннем строении оставался открытым. Конец 18 века был отмечен таким знаменательным событием в научном мире, как открытие Д. И. Менделеевым периодической системы химических элементов. Это стало по-настоящему мощным прорывом того времени и приоткрыло завесу над пониманием того, что все атомы имеют единую природу, что они родственны друг другу. В дальнейшем, в 19 веке, еще одним важным шагом на пути к разгадке строения атома стало доказательство того, что в составе любого из них присутствует электрон. Работа ученых этого периода подготовила благодатную почву для открытий 20-го века.

Эксперименты Томсона
Английский физик Джон Томсон в 1897 году доказал, что в состав атомов входят электроны с отрицательным зарядом. На этом этапе ложные представления о том, что атом - предел делимости любого вещества, были окончательно разрушены. Как же Томсон сумел доказать существование электронов? Ученый в своих опытах помещал в сильно разреженные газы электроды и пропускал электрический ток. В результате возникали катодные лучи. Томсон тщательно изучил их особенности и обнаружил, что они являются потоком заряженных частиц, которые движутся с огромной скоростью. Ученый сумел высчитать массу этих частиц и их заряд. Он также выяснил, что их нельзя преобразовать в нейтральные частицы, поскольку электрический заряд - это основа их природы. Так были Томсон является и создателем первой в мире модели строения атома. Согласно ей, атом - это сгусток положительно заряженной материи, в которой равномерно распределены отрицательно заряженные электроны. Такое строение объясняет общую нейтральность атомов, так как противоположные заряды уравновешивают друг друга. Опыты Джона Томсона стали неоценимо важными для дальнейшего изучения строения атома. Однако многие вопросы оставались без ответа.

Исследования Резерфорда
Томсон открыл существование электронов, но он не сумел найти в атоме положительно заряженных частиц. исправил это недоразумение в 1911 году. Во время экспериментов, изучая активность альфа-частиц в газах, он обнаружил, что в атоме присутствуют частицы, положительно заряженные. Резерфорд увидел, что при прохождении лучей сквозь газ или через тонкую металлическую пластину происходит резкое отклонение незначительного количества частиц от траектории движения. Их буквально отбрасывало назад. Ученый догадался, что такое поведение объясняется столкновением с положительно заряженными частицами. Такие эксперименты позволили физику создать модель строения атома Резерфорда.

Планетарная модель
Теперь представления ученого несколько отличались от предположений, высказанных Джоном Томсоном. Разными стали и их модели атомов. позволил ему создать совершенно новую теорию в этой области. Открытия ученого имели решающее значение для дальнейшего развития физики. Модель Резерфорда описывает атом как ядро, расположенное в центре, и движущиеся вокруг него электроны. Ядро обладает положительным зарядом, а электроны - отрицательным. Модель атома по Резерфорду предполагала вращение электронов вокруг ядра по определенным траекториям - орбитам. Открытие ученого помогло объяснить причину отклонения альфа-частиц и стало толчком к развитию ядерной теории атома. В модели атома Резерфорда прослеживается аналогия с движением планет Солнечной системы вокруг Солнца. Это очень точное и яркое сравнение. Поэтому модель Резерфорда, атом в которой движется вокруг ядра по орбите, была названа планетарной.

Работы Нильса Бора
Двумя годами позже датский физик Нильс Бор попытался объединить представления о строении атома с квантовыми свойствами светового потока. Ядерная модель атома Резерфорда была положена ученым в основу его новой теории. По предположению Бора, атомы вращаются вокруг ядра по круговым орбитам. Такая траектория движения приводит к ускорению электронов. Кроме того, кулоновское взаимодействие этих частиц с центром атома сопровождается созданием и расходованием энергии для поддержания пространственного электромагнитного поля, возникающего из-за движения электронов. При таких условиях отрицательно заряженные частицы должны когда-нибудь упасть на ядро. Но этого не происходит, что указывает на большую устойчивость атомов как систем. Нильс бор понял, что законы классической термодинамики, описанные уравнениями Максвелла, не работают во внутриатомных условиях. Поэтому ученый поставил перед собой задачу вывести новые закономерности, которые были бы справедливы в мире элементарных частиц.

Постулаты Бора
Во многом благодаря тому, что существовала модель Резерфорда, атом и его составляющие были неплохо изучены, Нильс Бор смог подойти к созданию своих постулатов. Первый из них гласит о том, что атом имеет при которых он не изменяет свою энергию, а электроны при этом движутся по орбитам, не меняя своей траектории. Согласно второму постулату, при переходе электрона с одной орбиты на другую происходит выделение или поглощение энергии. Она равна разности энергий предшествующего и последующего состояний атома. При этом, если электрон перепрыгивает на более близкую к ядру орбиту, то происходит излучение и наоборот. Несмотря на то что движение электронов мало напоминает орбитальную траекторию, расположенную строго по окружности, открытие Бора позволило получить великолепное объяснение существованию линейчатого спектра Приблизительно в это же время ученые-физики Герц и Франк, жившие в Германии, подтвердили учение Нильса Бора о существовании стационарных, стабильных состояний атома и возможность изменения значений атомной энергии.

Сотрудничество двух ученых
Кстати, Резерфорд длительное время не мог определить Ученые Марсден и Гейгер попытались осуществить перепроверку утверждений Эрнеста Резерфорда и в результате подробных и тщательных экспериментов и расчетов пришли к выводу о том, что именно ядро является важнейшей характеристикой атома, и в нем сосредоточен весь его заряд. В дальнейшем было доказано, что значение заряда ядра численно равно порядковому номеру элемента в периодической системе элементов Д. И. Менделеева. Интересно, что Нильс Бор вскоре познакомился с Резерфордом и полностью согласился с его взглядами. В последующем ученые длительно работали вместе в одной лаборатории. Модель Резерфорда, атом как система, состоящая из элементарных заряженных частиц, - все это Нильс Бор посчитал справедливым и навсегда отложил в сторону свою электронную модель. Совместная научная деятельность ученых была очень успешной и принесла свои плоды. Каждый из них углубился в изучение свойств элементарных частиц и сделал значимые для науки открытия. Позже Резерфорд обнаружил и доказал возможность разложения ядра, но это уже тема другой статьи.
Первая попытка создания модели атома была предпринята Дж. Томпсоном. Он полагал, что атом – это электронейтральная система формы шара с радиусом 10 - 10 м. На рисунке 6 . 1 . 1 . показано, как одинаково распределяется положительный заряд атома, причем отрицательные электроны располагаются внутри него. Чтобы получить объяснение линейчатых спектров атомов, Томпсон тщетно пытался определить расположение электронов в атоме, для расчета частоты их колебаний в положении равновесия. Спустя время Э. Резерфорд доказал, что заданная Томсоном модель была неверна.
Рисунок 6 . 1 . 1 . Модель Дж. Томпсона .
Внутренняя структура атомов была исследована Э. Резарфордом, Э. Марсденом, Х. Гейгером еще в 1909 - 1911 годах. Было применено зондирование атома α -частицами, возникающими во время радиоактивного распада радия и других элементов. Их масса в 7300 раз больше массы электрона, а положительный заряд равняется удвоенному элементарному заряду.
В опытах Резерфорда были использованы α -частицы, имеющие кинетическую энергию 5 М э в.
Определение 1
Альфа-частицы – это ионизированные атомы гелия.
Когда было изучено явление радиоактивности, этими частицами Резерфорд уже «бомбардировал» атомы тяжелых металлов. Входящие в них электроны не могут заменить траектории α -частиц, так как имеют малый вес. Рассеяние может быть вызвано тяжелой положительно заряженной частью атома. На рисунке 6 . 1 . 2 подробно описан опыт Резерфорда.

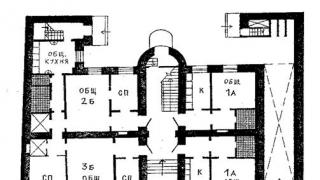
Рисунок 6 . 1 . 2 . Схема опыта Резерфорда по рассеянию α -частиц. K – свинцовый контейнер с радиоактивным веществом, Э – экран, покрытый сернистым цинком, Ф – золотая фольга, M – микроскоп.
Радиоактивный источник, заключенный в свинцовый контейнер, располагается таким образом, что
α
-частицы направляются от него к тонкой металлической фольге. Рассеянные частицы попадают на экран со слоем кристаллов сульфида цинка, светящиеся от их ударов. Сцинтилляции (вспышки) можно наблюдать при помощи микроскопа. Угол φ к первоначальному направлению пучка не имеет ограничений для данного опыта.
После испытаний было выявлено, что α -частицы, проходящие через тонкий слой металла, не испытывали отклонений. Наблюдались их отклонения и на углы, превышающие 30 градусов и близкие к 180 .
Результат Резерфорда противоречил модели Томпсона, так как положительный заряд не был распределен по всему объему атома. Согласно модели Томпсона, заряд не имеет возможности создавать сильное электрическое поле, которое впоследствии отбросит α -частицы. Такое поле однородно заряженного шара максимально на его поверхности и убывает до нуля к центру.
Определение 2
При уменьшении радиуса шара с положительным зарядом атома максимальная сила отталкивания, действующая на α -частицы, по закону Кулона увеличилась бы в n 2 раз.
Если размеры α - частиц достаточно большие, тогда рассеивание может достичь угла в 180 градусов.
Определение 3
Резерфорд пришел к выводу, что пустота атома связана с наличием положительного заряда, сосредоточенного в малом объеме. Данная часть была названа атомным ядром .

Рисунок 6 . 1 . 3 . Рассеяние α -частицы в атоме Томсона (a) и в атоме Резерфорда (b) .
Резерфорд выяснил, что центр атома имеет положительно заряженное ядро с диаметром 10 - 14 - 10 - 15 м. Оно занимает 10 - 12 полного объема атома, но содержит весь положительный заряд и около 99 , 95 % его массы. Вещество, входящее в состав атома, предполагало наличие плотности p ≈ 10 15 г / с м 3 , а заряд ядра равнялся суммарному заряду электронов. Было установлено, что при взятии за 1 значение заряда электрона, заряд ядра равнялся числу из таблицы Менделеева.
Опыты Резерфорда приводили к радикальным выводам и сомнениям ученых. Используя классическое представление о движении микрочастиц, он предлагает планетарную модель атома. Ее смысл заключался в том, что центр атома состоит из положительно заряженного ядра, которое является основной частью массы элементарной частицы. Атом считается нейтральным. При наличии кулоновских сил вокруг ядра по орбиталям вращаются электроны, как показано на рисунке 6 . 1 . 4 . Электроны всегда находятся в состоянии движения.

Рисунок 6 . 1 . 4 . Планетарная модель атома Резерфорда. Показаны круговые орбиты четырех электронов.
Предложенная Резерфордом планетарная модель была толчком в развитии знаний о строении атома. Благодаря ей, опыты по рассеиванию α -частиц смогли объяснить. Но вопрос об его устойчивости остался открытым. Исходя из закона классической электродинамики, заряд, движущийся с ускорением, излучает электромагнитные волны, забирающие и распределяющие энергию. За время 10 - 8 с все электроны потратить всю энергию, вследствие чего упасть на ядро. Так как это не происходит, есть объяснение – внутренние процессы не выполняются согласно классическим законам.
Если вы заметили ошибку в тексте, пожалуйста, выделите её и нажмите Ctrl+Enter
1903 году Дж. Дж. Томсон , предложил модель атома, согласно которой атом представляет собой сферу, равномерно заполненную положительным электричеством. Электроны погружены в эту среду и взаимодействуют с элементами этой среды по закону Кулона (рис. 4.1, а ). Согласно этой модели атом в целом нейтрален: суммарный заряд сферы и заряда электронов равен нулю.
Спектр такого атома должен был быть сложным, но никоим образом не линейчатым, что противоречило экспериментальным данным. По модели Томсона колеблющийся электрон (осциллятор) может испускать электромагнитную волну. При отклонении электрона от положения равновесия возникают силы, которые стремятся возвратить его в положение равновесия. Благодаря этому возникают колебания электрона, которые обусловливают излучение атома.
Была предложена также модель атома, изображенная на рис. 4.1,б : атом состоял из сферы, в центре которой находилось положительно заряженное ядро, а вокруг него располагались электроны. Однако и эта модель не смогла объяснить результаты экспериментов.
Наиболее известна планетарная модель атома, предложенная английским физиком Э. Резерфордом (рис. 4.1, в).
Первые эксперименты по изучению строения атома были выполнены Э. Резерфордом и его сотрудниками Э. Марсденом и Х. Гейгером в 1909-1911 годах. Резерфорд предложил применить зондирование атома с помощью α -частиц, которые возникают при радиоактивном распаде радия и некоторых
а б в
других элементов. Эти опыты стали возможны благодаря открытию явления радиоактивности, при котором в результате естественного радиоактивного распада тяжелых элементов выделяются - частицы, имеющие положительный заряд, равный заряду двух электронов, масса - частицы в 4 раза больше массы атома водорода, т.е. они являются ионами атома гелия . Энергия -частиц, испускаемых различными тяжелыми химическими элементами, изменяется от эВ для урана до эВ для тория. Масса α -частиц примерно в 7300 раз больше массы электрона, а положительный заряд равен удвоенному элементарному заряду. В этих опытах использовались α -частицы с кинетической энергией 5 МэВ , что соответствовало их скорости около м/с .
Эти частицы бомбардировали фольги из тяжелых металлов (золото, серебро, медь и др.). Электроны, входящие в состав атомов, вследствие малой массы не изменяют траекторию α -частицы. Рассеяние, то есть изменение направления движения α -частиц, может вызвать только тяжелая положительно заряженная часть атома.
Цель опытов Резерфорда состояла в том, чтобы экспериментально проверить основные положения модели атома, предложенной Томсоном.
Схема опыта Резерфорда по рассеянию α -частиц показана на рис. 4.2.
Здесь K - свинцовый контейнер с радиоактивным веществом, Э - экран, покрытый сернистым цинком, Ф - золотая фольга, M - микроскоп. От радиоактивного источника, заключенного в свинцовый контейнер, α -частицы направлялись на тонкую металлическую фольгу. Толщина фольги составляла м (1 мкм ), что эквивалентно примерно 400 слоям из атомов золота. Рассеянные фольгой α -частицы попадали на экран, покрытый слоем кристаллов сульфида цинка, способных светиться под ударами быстрых заряженных частиц. Сцинтилляции (вспышки) на экране наблюдались глазом
С помощью микроскопа. Микроскоп и связанный с ним экран можно было вращать вокруг оси, проходящей через центр фольги. Т.е. можно было всегда измерить угол отклонения α -частиц от прямолинейной траектории движения. Весь прибор помещался в вакуум, чтобы α -частицы не рассеивались при столкновении с молекулами воздуха.
Наблюдения рассеянных α -частиц в опыте Резерфорда можно было проводить под различными углами φ к первоначальному направлению пучка. Было обнаружено, что большинство α -частиц проходило через тонкий слой металла, практически не испытывая отклонения. Однако небольшая часть частиц все же отклонялась на значительные углы, превышающие 30°. Очень редкие α -частицы (приблизительно одна на десять тысяч) испытывали отклонение на углы, близкие к 180°. Этот результат был неожиданным, т.к. находился в противоречии с моделью атома Томсона, согласно которой положительный заряд распределён по всему объёму атома.
При таком распределении положительный заряд не может создать сильное электрическое поле, способное отбросить α -частицы назад. Электрическое поле однородного заряженного шара максимально на его поверхности и убывает до нуля по мере приближения к центру шара. Если бы радиус шара, в котором сосредоточен весь положительный заряд атома, уменьшился в n раз, то максимальная сила отталкивания, действующая на α-частицу по закону Кулона, возросла бы в n 2 раз. Тогда при достаточно большом значении n α -частицы могли бы испытать рассеяние на большие углы вплоть до 180°. Эти соображения привели Резерфорда к выводу, что атом почти пустой, и весь его положительный заряд сосредоточен в малом объёме, имеющем размеры порядка
10 -14 м . Эту часть атома Резерфорд назвал атомным ядром . Электроны, по мнению Резерфорда, движутся вокруг ядра с размерами порядка 10 -14 м . Так возникла ядерная модель атома (рис. 4.1, в ).
На основании полученных результатов Резерфорд, учитывая, что электроны атома не могут существенно влиять на рассеяние относительно тяжелых и быстрых -частиц, сделал выводы, которые были положены в основу планетарной (ядерной) модели атомов:
1) существует ядро, в котором сосредоточена вся масса атома и весь его положительный заряд, причем размеры ядра значительно меньше, чем размер самого атома;
2) электроны, которые входят в состав атома, движутся вокруг ядра по круговым орбитам.
Исходя из этих двух предпосылок и предполагая, что взаимодействие между налетающей -частицей и положительно заряженным ядром определяется кулоновскими силами, Резерфорд установил, что атомные ядра имеют размеры м , т.е. они в раз меньше размеров атомов. Ядро занимает только 10 -12 часть полного объёма атома, но содержит весь положительный заряд и не менее 99,95 % его массы. Вещество, составляющее ядро атома, имеет колоссальную плотность ρ≈10 17 кг /м 3 . Заряд ядра должен быть равен суммарному заряду всех электронов, входящих в состав атома.
Впоследствии удалось установить, что если заряд электрона принять за единицу, то заряд ядра в точности равен номеру данного элемента в таблице Менделеева. Величина положительного электрического заряда атомного ядра Z определяется количеством протонов в ядре (и, следовательно, количеством электронов в атомных оболочках), которое совпадает с порядковым номером элемента в периодической таблице. Заряд равен Zе , где е = 1,602 · 10 -19 Кл - абсолютная величина элементарного электрического заряда. Заряд определяет химические свойства всех изотопов данного элемента.
В 1911 Резерфорд, используя закон Кулона, получил формулу
где N - количество α -частиц, падающих в единицу времени на рассеиватель; dN - количество рассеянных в единицу времени α -частиц в телесном угле dΩ под углом θ ; Ze и n - заряд ядер рассеивателя и их концентрация; dx − толщина слоя фольги; V и m α - скорость и масса α -частиц.
Прямые опыты по измерению заряда ядер на основе формулы Резерфорда были выполнены Чедвиком в 1920 году. Схема опыта Чедвика приведена на рис. 4.3.
Рассеиватель в виде кольца (заштриховано на рис. 4.3) размещался соосно и на равных расстояниях между источником И и детектором α -частиц Д. При измерении количества dN рассеянных α-частиц отверстие в кольце закрывалось экраном, который поглощал прямой пучок α-частиц из источника
в детектор. Детектор регистрировал только α -частицы, рассеянные в телесном
угле dΩ под углом θ к падающему пучку α -частиц. Затем кольцо перекрывалось экраном с отверстием, и измерялась плотность тока α -частиц в точке расположения детектора. По полученным данным, рассчитывали количество N α -частиц, падающих на кольцо в единицу времени. Таким образом, если известна энергия α - частиц, испускаемых источником, без труда определялась величина Z в формуле (4.1).
Формула Резерфорда позволила объяснить экспериментальные результаты по рассеянию α -частиц на тяжелых ядрах, что привело к открытию атомного ядра и созданию ядерной модели атома.
Модель атома, предложенная Резерфордом, напоминает Солнечную систему. Именно поэтому модель Резерфорда получила название планетарной модели атома. Эта модель стала значительным шагом на пути к современным представлениям о строении атома. Лежащее в ее основе понятие атомного ядра, в котором сосредоточены весь положительный заряд атома и практически вся его масса, сохранило свое значение до настоящего времени.
Однако, в отличие от планетарной модели Солнечной системы, планетарная модель атома оказывается внутренне противоречивой с точки зрения классической физики. И это, прежде всего, связано с наличием у электрона заряда. Согласно законам классической электродинамики вращающийся вокруг ядра электрон, как и любая ускоренно движущаяся заряженная частица, будет излучать электромагнитные волны. Спектр такого излучения должен быть непрерывным, то есть содержать электромагнитные волны с любой длиной волны. Уже этот вывод противоречит линейчатости спектров излучения атомов, наблюдаемой на опыте.
Кроме того, непрерывное излучение уменьшает кинетическую энергию электрона. Поэтому, за счет излучения радиус орбиты движущегося электрона обязан уменьшаться, и, в конце концов, электрон должен упасть на ядро, как показывают оценки, за время . Однако в действительности атом водорода является устойчивой и «долгоживущей» электромеханической системой. Иными словами, планетарная модель атома с точки зрения классической физики оказывается неустойчивой.
В начале XXв. опытами по облучению тонкой фольги α-частицами Э. Резерфорд определил структуру атома. Он показал, что атом имеет планетарную модель (рис. 3), то есть состоит из плотного положительно заряженного ядра, вокруг которого обращается рыхлая электронная оболочка.
Рис. 3. Планетарная модель строения атома Э. Резерфорда
В целом атом является электронейтральной элементарной структурой химического элемента. Физический смысл порядкового номера Z-элемента в периодической системе элементов был установлен в планетарной модели атома Резерфорда. Z совпадает с числом положительных элементарных зарядов в ядре, закономерно возрастающих на единицу при переходе от предыдущего элемента к последующему. Химические свойства элементов и ряд их физических свойств объясняются поведением внешних, так называемых валентных электронов их атомов.
Поэтому периодичность свойств химических элементов должна быть связана с определенной периодичностью в расположении электронов в атомах различных элементов. Теория периодической системы основывается на следующих положениях:
а) порядковый номер химического элемента равен общему числу электронов в атоме данного элемента;
б) состояние электронов в атоме определяется набором их квантовых чисел п, l , m и m s . Распределение электронов в атоме по энергетическим состояниям должно удовлетворять принципу минимума потенциальной энергии: с возрастанием числа электронов каждый следующий электрон должен занять возможное энергетическое состояние с наименьшей энергией;
в) заполнение электронами энергетических состояний в атоме должно происходить в соответствии с принципом Паули.
Электроны в атоме, занимающие совокупность состояний с одинаковым значением главного квантового числа п , образуют электронную оболочку, или электронный слой. В зависимости от значенийn различают следующие оболочки:К прип = 1,L прип = 2,М приn = 3,N прип = 4,О прип = 5 и т. д. Максимальное число электронов, которые могут находиться в оболочках согласно принципу Паули: вК -оболочке – 2 электрона, в оболочкахL ,М ,N иО соответственно 8, 18, 32 и 50 электронов. В каждой из оболочек электроны распределяются по подгруппам или подоболочкам, каждая из которых соответствует определенному значению орбитального квантового числа. В атомной физике принято обозначать электронное состояние в атоме символомп l , указывающим значение двух квантовых чисел. Электроны, находящиеся в состояниях, характеризуемых одинаковыми квантовыми числамиn иl , называются эквивалентными. ЧислоZ -эквивалентных электронов указывается показателем степени в символеnl z . Если электроны находятся в некоторых состояниях с определенными значениями квантовых чиселп иl , то считается заданной так называемая электронная конфигурация. Например, основное состояние атома кислорода можно выразить следующей символической формулой: 1s 2 , 2s 2 , 2p 4 . Она показывает, что два электрона находятся в состояниях сn = 1 иl = 0, два электрона имеют квантовые числаn = 2 иl = 0 и четыре электрона занимают состоянияc n = 2 иl = 1.
Порядок заполнения электронных состояний в оболочках атомов, а в пределах одной оболочки – в подгруппах (подоболочках) должен соответствовать последовательности расположения энергетических уровней с данными п иl . Сначала заполняются состояния с наименьшей возможной энергией, а затем состояния со все более высокой энергией. Для легких атомов этот порядок соответствует тому, что сначала заполняется оболочка с меньшимп и лишь затем должна заполняться электронами следующая оболочка. В пределах однойоболочки сначала заполняются состояния с l = 0, а затем состояния с большими l , вплоть доl =п – 1. Взаимодействие между электронами приводит к тому, что для достаточно больших главных квантовых чиселn состояния с большимn и малымl могут иметь меньшую энергию, то есть быть энергетически более выгодными, чем состояния с меньшимп , но с большимl . Из изложенного следует, что периодичность химических свойств элементов объясняется повторяемостью электронных конфигураций во внешних электронных подгруппах у атомов родственных элементов.